Co mają wspólnego ciasteczka owsiane ze zjawiskami fizycznymi i reakcjami chemicznymi oraz układem okresowym pierwiastków chemicznych?
W atmosferze bakaliowych zapachów, na to pytanie i wiele innych, próbowali odpowiedzieć uczniowie klas siódmych podczas lekcji chemii.
Ciasteczka owsiane to super przepis sam w sobie, jak i baza do dalszych eksperymentów chemicznych. Możecie do nich dorzucić ulubione bakalie, orzechy czy wiórki kokosowe, dużą łyżkę masła orzechowego, posiekane migdały. Poddane obróbce składniki kontaktują się z tlenem z powietrza a przez to ulegają reakcji utleniania, szczególnie intensyfikowanej przez podwyższenie temperatury i rozwijanie powierzchni przez rozdrabnianie i mieszanie.
Jak już opanujecie konsystencję, to możecie kombinować do woli! Koniecznie dajcie znać, czy jakoś je udoskonaliliście.

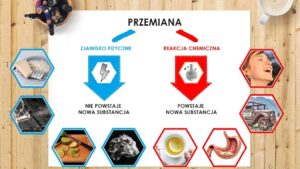
Pamiętaj! Zjawisko fizyczne to przemiana, w której nie powstaje nowa substancja, natomiast reakcja chemiczna to reakcja w której powstaje nowa substancja.
Polecenie 1
Najczęściej stosowanym spożywczym środkiem spulchniającym jest wodorowęglan sodu (soda oczyszczona) NaHCO3, który podczas ogrzewania ulega rozkładowi, w wyniku reakcji chemicznej. Zjawisko to zachodzi podczas pieczenia ciasta, co można opisać równaniem chemicznym:
2NaHCO3 → Na2CO3 + H2O + CO2
Oblicz ile gramów CO2 może się wydzielić jeżeli do pieczonego ciasta użyto całego opakowania środka spulchniającego o gramaturze 50 g?
Pamiętaj jednak, że średnio używa się 1 łyżeczkę sody oczyszczonej (około 5 g) na 500 g mąki, tak aby w cieście nie powstało zbyt dużo węglanu sodu Na2CO3, ponieważ substancja nadaje potrawom nieprzyjemny posmak.
Ile mąki należy użyć do upieczenia tego ciasta, aby nie miało nieprzyjemnego posmaku?
Jeżeli masz problem, jak rozwiązać zadanie, skorzystaj z podpowiedzi:
z równania wynika, że ze 168 g NaHCO3 można otrzymać 44 g CO2.
Dorota Gawron
nauczyciel chemii












